Covid-19
|
Magnus Westgren, professor, ME Graviditet och förlossning, Karolinska Universitetssjukhuset Karin Pettersson, docent, överläkare, BB Stockholm Lars Navér, docent, överläkare, ME Neonatologi, Astrid Lindgrens Barnsjukhus Marie Studahl, docent, överläkare, Infektion Sahlgrenska Universitetssjukhuset/Östra |
- Introduktion
- Agens
- Smittsamhet och spridning i befolkningen och i samhället
- Klinisk bild
- Infektion hos den gravida kvinnan
- Infektion hos fostret och det nyfödda barnet
- Överföringsrisk
- Laboratoriemetoder
- Diagnos av moderns infektion
- Undersökning av placenta
- Diagnos av fostrets/barnets infektion
- Profylax
- Terapi
- Svenska erfarenheter
- Handläggning
- Referenser
- Introduktion
Kunskapsutvecklingen inom området går mycket snabbt. För att få med den mest aktuella informationen finns länkar till olika smittskyddsenheter världen över som uppdaterar tillgänglig information ofta samt referenser till relevanta publikationer. Särskilt myndigheter.
Under avsnittet Handläggning finns aktuell rekommendation från SFOG och neonatalföreningen.
Vi går ofta igenom länkarna för att se att de fungerar. Men myndigheter och tidskrifter ändrar ofta sina hemsidor varför adresserna kan ändras. Därför anges inte bara länken utan även namnet på avsnittet så att man då kan söka sig fram till sökt information. Skulle något inte fungera är vi tacksamma om ni rapporterar det till oss via mail infpreg.karolinska@sll.se.
- Agens
Covid-19 orsakas av ett tidigare okänt humant coronavirus SARS-CoV-2 (severe acute respiratory syndrome coronavirus-2). Coronavirusfamiljen omfattar många stora höljeförsedda RNA virus som i elektronmikroskopet ser ut som en krona därav namnet. De flesta coronavirus finns i djurvärlden.
CoronavirusInom humanmedicin var sex stammar kända sedan tidigare. Fyra cirkulerar ständigt och ingår i den luftvägsflora som orsakar en stor del av ”vanliga” förkylningssjukdomar och har ägnats ganska liten uppmärksamhet. Två andra mycket patogena stammar har tidigare orsakat allvarliga epidemier med svåra nedre luftvägsinfektioner: SARS-CoV-1 (severe acute respiratory syndrome) spreds från södra Kina till närliggande länder 2002-2003 (kring 8000 fall, 750 kända dödsfall) men spreds inte vidare och har inte påvisats sedan dess. MERS-CoV (middle east respiratory syndrome) (enligt WHO 2519 kända fall, 866 dödsfall) på Arabiska halvön 2012-2013. MERS-CoV cirkulerar fortfarande på Arabiska halvön men endast få fall identifieras årligen.
Dessa två och SARS-CoV-2 (”emerging viruses”) har sannolikt liksom många andra coronavirus överförts från djurvärlden. Sådana hopp förekommer frekvent och är oftast utan betydelse. Men när ett sådant virus blir patogent och mycket smittsamt sprids det snabbt i en befolkning som är helt mottaglig och kan orsaka en pandemi som den nu pågående.
Jämförande studier över virus RNA sekvens pekar på att någon av många coronavirus-stammarna hos fladdermöss kan vara ursprung till dessa tre farliga humanpatogena coronavirus men med olika mellanvärdar: för MERS-CoV sannolikt kamel, för SARS-CoV-1 ett mårddjur. Virusvarianter har sedan anpassats till människa. För SARS-CoV-2 har mellanvärd ännu inte kunnat fastställas. En obekräftad teori är att SARS-CoV-2 kan ha spritts från levande djur till människor på marknad i staden Wuhan i Hubei provinsen i Kina i slutet av 2019.
SARS-CoV-2Den nya virusstammen SARS-CoV-2 kan orsaka allvarlig sjukdom men i avsevärt lägre omfattning än de två föregångarna. Men SARS-CoV-2 virus är mer smittsamt och sprids mycket snabbt när alla eller största delen av befolkningen saknar immunitet. Även om virusinfektionen medför låg risk för den enskilda individen blir det, om ett mycket stort antal individer smittas, många särskilt bland de med svagheter p.g.a. andra sjukdomar och/eller ålder, som blir svårt sjuka och kan dö om smittspridningen inte kan stoppas.
SARS-CoV-2 isolerades och identifierades i Kina som ett nytt coronavirus. Genomets RNA sekvens offentliggjordes den 7 januari 2020. Världen över omdirigerades stora kompetens- och ekonomiska resurser och intensivt arbete pågår för att snabbast möjligt skaffa verktyg för att bekämpa pandemin: storskalig virusdiagnostik, karakterisering av nya virusvarianter, verksamma antivirala medel och vaccin för att nämna några hörnstenar.
Virus egenskaper kartlades: höljet med de utskjutande ”spikarna” är nödvändiga för att virus ska vara infektiöst. I spikarnas ytterända finns ett protein som binds till receptorn ACE2 (angiotensinkonvertas-2) och sedan måste klyvas av ett enzym, serinproteas TMPRSS2 innan virus kan tränga in i cellerna och föröka sig. ACE2 och TMPRSS2 finns på luftvägarnas epitelceller, alveoler, blodkärlens endotelceller där också virus förökar sig. ACE2 receptor uttrycks även på epitelceller i tarm, njure.
MutationerSyntes av nya viruspartiklar sker sedan inne i cellen. RNA-genomet i coronavirus är stort (cirka 30 000 baspar). Vid nybildningen av RNA genom kan felläsning ske - ordningen på baserna byts ut eller baser uteblir (deletioner). Kontrollfunktioner finns som hindrar att större delar av genomet byts ut (vilket sker ex vis vid influensa). För SARS-CoV-2 sker mutationerna förhållandevis långsamt med enstaka förändringar när virus sprids från en person till en annan eller under förloppet hos en långvarigt svårt sjuk individ. Men passage av virus från person till person har redan skett många hundratals miljoner gånger!
De flesta mutationer är till nackdel för virus och försvinner eller är tysta dvs de förändrar inte egenskaper hos virus - men kan i smittspårningsarbetet utnyttjas för att söka smittvägar.
Men om mutationer sker i den genetiska koden för viktiga virusstrukturer i t ex spike proteinet och/eller andra angreppspunkter för kroppens immunförsvar kan viktiga ytegenskaper förändras. Och det immunförsvar som byggts mot tidigare virusvariant eller med vaccin kan bli mindre verksamt mot smitta med de nya varianterna. Virusmutanter bäst anpassade för att spridas tar över och smittmönster ändras.
Mutationer kan även leda till mer patogena stammar. Det skulle emellertid innebära nackdel för spridning av virus och under andra virusepidemier har man snarare sett en förändring mot minskad svårighetsgrad. Men utvecklingen vid nu pågående pandemi kan inte förutses och måste följas noggrant.
Bevakning av muterade stammar har utökats och blir viktigare ju längre vaccinationsprogrammen fortskrider. Likartade mutationer kan uppstå i olika delar av världen men rapporteras där bevakning och sekvensbestämning av cirkulerande stammar är mest adekvat. Ett ständigt stigande antal (flera 100 000-tals) sekvenserade SARS-CoV-2 genom registreras i en databas allmänt tillgänglig på internet.
Variants of concern - VOC (se WHO här)Fem spridda mutanter har av WHO hittills förklarats vara "variants of concern" - dvs mutanter med potential att medföra ny smittvåg. De är under bevakning för att spåra ändringar i smittmönster, sjukdomsgrad och minskad effekt av immunitet förvärvad genom infektion med tidigare varianter eller vaccination.
Enl WHO benämns VOC med grekiska bokstäver. De nu aktuella är omikron med subvarianter BA1-5 (VOC sedan nov 2021). Tidigare VOC, orsak till omfattande smittvågor: alfa och beta (dec 2020-mars 2021), gamma (jan 2021- september 2021), delta maj 2021- december 2021) har nu tagits bort från VOC listan då de inte cirkulerar längre.
I Sverige dominerade den första smittvågen våren 2020 av Wuhan - likt virus, den andra vågen senhöst 2020-vår 2021 av alfa varianten, våren 2021 även beta. Efter det tog delta över i en tredje våg. Omikron mutanten kom i slutet av 2021 och har snabbt ersatt deltavarianten (här i december 2021). För vidare epidemiologi här och i Europa se FoHM och ECDC.
Alfa och delta-varianten orsakade något högre andel allvarlig sjukdom än den ursprungliga Wuhan varianten. Omikronvarianterna förefaller inte infektera lungepitelceller lika effektivt som deltavarianten men väl där kan sjukdomen hos ovaccinerade bli lika svår som med deltavarianten. Stora mängder omikron virus bildas i övre luftvägarna - smittsamheten kan vara mycket hög,
Omicron mutanter har från slutet av 2021 snabbt svept över världen och dominerar nu helt den stora smittspridning, som först nu (april 2022) förefaller minska (se FoHM. och ECDC). Omikronvirus och de subvarianter, som februari 2022 tagit över (BA.2 - nu BA5 varianter), har ett mycket stort antal mutationer i den del av spike-proteinet som binder till antikroppar och respiratoriskt epitel. Detta medför 1. något minskat skydd av befintliga SARS-CoV2 antikroppar 2. ökad produktion av virus i övre luftvägarna = hög smittsamhet 3. kortare inkubationstid, 4.barn i allt yngre åldrar infekteras - sjuknar Det cellbundna försvaret är mindre påverkat, vilket stämmer väl med att minst två - framför allt tre eller fyra - doser av befintliga mRNA vaccin ger mycket gott skydd mot svår sjukdom/död däremot inte mot ytlig reinfektion/smittsamhet. Detta driver smittspridningen.
mRNA vaccin inkluderande de tidiga omikronvarianterna finns framtagna och utprövade. De bLEVi tillgängliga under hösten 2022. Vaccinskyddet mot svår sjukdom breddas och fördjupas men skyddet mot vidaresmitta med de nya omikronvarianterna är ännu inte känt.Ännu vet man inte om vaccinskyddet med andra covid-19 vaccin kan vara mindre känsligt för mutationer t ex ”konventionellt” helvirionvaccin eller något av det 60-tal lovande vaccinkandidater som bygger på olika principer och är långt framme i fas I-III utprövning. Målet är att få fram vaccin som skyddar mot alla coronavirus för att hindra nya coronviruspandemier i framtiden.
Smittförekomst
Hos infekterade personer utsöndras virus i utandningsluften - störst mängd hos de svårt sjuka - och kan finnas i blod/serum, urin, avföring och svett. Virus är relativt stabilt på olika ytor under experimentella förhållanden timmar till dagar beroende på underlaget.
Eftersom virushöljet innehåller lipider förstörs det lätt av tvål och vatten, 70 % alkohol, vanliga alkoholbaserade yt-desinfektionsmedel, klorin, väteperoxid, diskmedel, tvättmedel.
- Smittsamhet och spridning i befolkningen och i samhället
Smittsamheten vid covid-19 är mycket hög. SARS-CoV-2 spreds därför snabbt över världen: ”a pneumonia of unknown cause detected in Wuhan, China” rapporterades den 31 december 2019 till WHO country office in China. Den 11 mars förklarade WHO att smittspridning var så omfattande att det rörde sig om en pandemi.
Även i Sverige var smittspridningen stor under våren 2020. Man försökte begränsa smittspridning med hjälp av smittförebyggande restriktioner och utökad provtagning/smittspårning. Efter en nedgång under sommaren 2020 ökade smittan återigen snabbt under luftvägsinfektions-säsongen 2020/21 (se FoHM här). mRNA-vaccin blev tillgängliga i början av 2021.Vaccinationer av en hög andel av befolkningen över 18 år har medfört gott skydd mot svår sjukdom och död: Trots en mycket stor smittspridning och ökning av lindriga infektioner med de nya omicron virusvarianterna under luftvägssäsongen 2021 - 22 har antalet sjukhus/intensivvårdade covidsjuka minskat (se statistik från Socialstyrelsen här) en stor andel av de som behövde sjukhusvård var ovaccinerade. Smittspridning var under våren 2022 på nedåtgående men fanns fortfarande allmänt i samhället - nya omikronvarianter har introducerats. Smittspridningen har stigit igen under hösten och ökade ytterligare under senhöst vintersäsong.
Genom att följa virus/antikroppsprevalens med jämna mellanrum fick man under prevaccinationsperioden ett reellt mått på smittspridningen i olika regioner och befolkningsgrupper (se Folkhälsomyndighetens hemsida). Mängden virus RNA i avloppsvatten är ett annat mått på smittspridningens omfattning och lokalisation. Resultaten ger vägledning för utformningen och effekten av strategiska åtgärder mot smittspridningen.
Observationsstudier med hjälp av nu allmänt tillgängliga systematiska testmöjligheter ger också en bild av smittsamheten och smittvägar vid covid-19:
- Enligt tidigare kunskap smittade covid-19 i första hand vid nära kontakter mellan personer genom så kallad droppsmitta. När en infekterad person nyser, hostar, talar, sjunger eller andas ut sprids små droppar till omgivningen. Smitta når längre vid högljutt tal och skratt, hojtande, sång än vid vanligt tal och är inomhus beroende på ventilation och luftströmmar särskilt i trängre utrymmen. Smitta med omikronvarianterna är sannolikt i högre grad luftburen.
- Aerosolsmitta förekommer t ex inom sjukvården vid vissa undersökningsmoment och vid behandling exvis från patienter som får syrgas via öppna system (se vidare Nationellt vårdprogram eller Smittskyddsläkareföreningens covid-19 läkarinfo).
- Smittan kan ta sig in i kroppen både via inandning eller genom direkt kontaktsmitta från smittförande sekret på händerna om man rör med nedsmittade händer i ögon eller på slemhinnor i näsa och mun. Handhygien av största betydelse.
- Virus finns ofta i tarmen och kan återfinnas i faeces hos infekterade individer, ibland längre tid än i luftvägarna. Hur stor roll det spelar för smittspridning är inte helt klart.
- Virus är relativt stabilt på ytor varför handöverförd smitta från handtag, ledstänger och andra ytor, som många ofta tar i, är möjlig. Omicron varianten har visats klara sig längre t ex på hud, plast och tyg än tidigare virusvarianter. Handhygien rekommenderas.
- Smittsamheten vid subklinisk infektion tidigare underskattad t ex på äldreboenden. Hos många subkliniskt infekterade individer är virusutsöndringen - mätt som virusnukleinsyra med mycket känslig PCR analys - låg och kan troligen vara mindre smittsamma. Men det gäller inte alla – somliga utsöndrar stora mängder virus och är mycket smittsamma.
Andelen subkliniskt infekterade kan skilja vid infektion med olika virusvarianter, vaccinationsgrad och i olika åldrar.
- Även den prekliniska utsöndringen kan variera med olika virusmutanter.
- Smittsamheten sannolikt störst vid symtomdebut och upp till 48 timmar tidigare och beräknas genomsnittligen vara några dagar efter det att patienten varit helt feberfri. Efter allvarlig sjukdom och hos immunsupprimerade kvarstår smittrisk avsevärt längre tid.
Från och med den 1 april 2022 är covid-19 inte längre klassad som samhällsfarlig sjukdom men är fortfarande anmälningspliktig.
FHM rekommenderar sedan 15 mars 2023 för allmänheten att person med symtom som vid covid-19 bör stanna hemma - gäller även vid negativt snabbtest - tills orken återvänder.
FHM rekommendation för vård och omsorg - Förebyggande åtgärder för covid-19 inom vård och omsorg Version 1, 2023-03-15 kan läsas här
Se även Nationellt vårdprogram covid19 här (snar uppdatering väntas)
- Enligt tidigare kunskap smittade covid-19 i första hand vid nära kontakter mellan personer genom så kallad droppsmitta. När en infekterad person nyser, hostar, talar, sjunger eller andas ut sprids små droppar till omgivningen. Smitta når längre vid högljutt tal och skratt, hojtande, sång än vid vanligt tal och är inomhus beroende på ventilation och luftströmmar särskilt i trängre utrymmen. Smitta med omikronvarianterna är sannolikt i högre grad luftburen.
- Klinisk bild
Inkubationstiden för varianterna som cirkulerade i början av pandemin var i median cirka 4-5 dagar, men varierade mellan 2-14 dagar. Omicron-varianten som dominerat i Sverige sedan november 2021 har kortare inkubationstid 3-4 dagar.
Infektionen kan vara asymtomatisk, vilket sannolikt är vanligt, men för närvarande är det okänt exakt hur vanligt det är.
Symtomatisk infektion kan ge allt från mild till måttlig eller svår och kritisk sjukdom. De flesta infektioner är milda, cirka 80 %.
Ålder spelar stor roll för den kliniska bilden, förloppet och risken att få svår sjukdom.
Hos vuxna är symtomen feber, trötthet, torrhosta, aptitlöshet, muskel-och ledvärk och andnöd. Febern kan vara allt från låggradig till hög. Symtom som huvudvärk, halsont, snuva, förlust av smak och lukt, illamående och diarré är också relativt vanligt förekommande.
Förloppet vid symtomatisk infektion kan vara allt från lindrigt till allvarligare. Vid mild sjukdom sker förbättring oftast inom en vecka, medan försämring kan ske hos individer med mer uttalade symtom. Det finns inga speciella kliniska symtom som med säkerhet kan skilja covid-19 från andra luftvägsinfektioner, annat än möjligtvis tilltagande dyspné flera dagar efter insjuknandet. Det är främst andnöden som för patienten till sjukhus och då vanligtvis efter 7- 8 dagars sjukdom.I början av pandemin när de tidiga virusvarianterna (alfa, beta, gamma, delta) spreds under 2020 och 2021 riskerade ca 15-20 % ovaccinerade att få svår sjukdom med kraftig andnöd och svårigheter att syresätta sig. En mindre andel (cirka 5%) fick kritisk sjukdom med respiratorisk svikt, chockbild och multiorgansvikt. Hos de som försämras har man identifierat ett svagt innat (dvs tidigt, medfött) immunsvar som därefter följs av kraftigt ökade akut fas-reaktanter och en dysreglering av immunsvaret. ARDS - acute respiratory distress syndrome kan utvecklas vilket ger lungsvikt vid kritisk covid-19 med vätskeutträde och inflammation i lungorna som försämrar syrgasupptaget. Vid svår sjukdom finns hjärtpåverkan såsom kardiomyopati och hjärtarytmier beskrivna, njursvikt är vanligt och upp till 30-40 % av intensivvårdade individer utvecklar tromboemboliska komplikationer (lungemboli, ventrombos, stroke). Neurologiska manifestationer förekommer, främst hos de svårast sjuka: encefalopati, hemorragiska lesioner och stroke men även mer ovanliga tillstånd finns beskrivna: meningoencefalit, hemorragisk encefalomyelit, Guillain-Barré syndrom och ADEM (akut disseminerad encefalomyelit).
Barn i alla åldrar kan få infektionen, men verkade bli smittade av alfa, beta, gamma, delta varianterna i lägre utsträckning än vuxna. Både spädbarn och barn smittas av omicronvarianten som dominerar i Sverige sedan december 2021. De får symtom med tecken på övre luftvägsinfektion och varierande grad av feber, torrhosta och rodnat svalg. De barn som behöver sjukhusvård är spädbarn som insjuknat och har svårigheter med vätskeintag/nutrition alternativt feberkramper. Större barn med riskfaktorer kan också behöva sjukhusvård. Det är mindre risk för allvarlig sjukdom, men hos en mycket liten andel av barn utvecklas ett inflammatoriskt tillstånd, med liknande symtom som vid Kawasakis sjukdom och toxic shock syndrome, vilket benämns Multisystem Inflammatory Disorder in Children and Adolescents (MIS-C).
Kliniskt kemiska analyser
Laboratoriemässigt ses vid måttlig/svår infektion oftast lymfopeni och neutrofili. Vidare ses förhöjda transaminaser och förhöjda akut fasreaktanter som CRP, ferritin, laktatdehydrogenas, D-dimer och procalcitonin. Vid svår sjukdom ses även förhöjda nivåer av protrombintid, troponin, kreatininkinas och kreatinin och dessa är associerade med sämre prognos. Hög D-dimer och uttalad lymfopeni har associerats till ökad mortalitet.
Radiologi
Datortomografi visar ”ground-glass -förändringar ” dvs. skyiga förtätningar igenom vilka kärl och bronker kan ses, överensstämmande med viral pneumonit. Förändringarna har beskrivits som övervägande bilaterala, med en perifer distribution och involverar nedre loberna. Även asymptomatiska personer och de med lindrig sjukdom kan ha förändringar på datortomografi. De radiologiska förändringarnas förekomst och utbredning är relaterade till ålder: yngre individer har mindre förändringar på datortomografi.
Riskfaktorer för svår sjukdom
Den viktigaste riskfaktorn för svår covid-19 är hög ålder, och personer över 70 år är den främsta riskgruppen. Men svår sjukdom kan drabba helt friska individer vid vilken ålder som helst. Allvarlig covid-19 drabbar företrädesvis vuxna i medelåldern eller personer i högre ålder med underliggande sjukdomar. Ungefär 75 -80% av sjukhusvårdade personer har en eller flera underliggande sjukdomar. Män är överrepresenterade bland de som får svår sjukdom. De sjukdomar som är överrepresenterade vid allvarlig sjukdom är:
o kardiovaskulär sjukdom ex. hjärtsvikt, kardiomyopati, koronarsjukdom
o diabetes mellitus typ 2
o kronisk njursjukdom
o fetma
o binjurebarksvikt
o kronisk obstruktiv lungsjukdom
o malignitet
o organtransplanterade
Mortalitet
Andelen som avlider av totala antalet infekterade individer (infection fatality ratio, IFR) är svår att fastställa eftersom många infektioner sannolikt är asymtomatiska eller ger mycket lindriga symtom, och därför inte blir diagnosticerade. Enligt Folkhälsomyndighetens beräkningar uppskattas infektionsdödligheten till 0,6 %. Andelen som avlider av verifierade fall varierar i olika åldersgrupper och mellan olika länder och är bl.a beroende av förekomsten av riskfaktorer i studierna, hur många som provtas och tidpunkten under pandemin som studien utfördes. Mortaliteten är dramatiskt högre i de äldre åldersgrupperna och det är större risk för män att avlida, medan risken är mycket låg (0.1%) hos personer yngre än 70 år.
Dödligheten var högre i början av pandemin och har successivt sjunkit främst vid tillgång till effektiva vaccin men också genom minskande patogenicitet hos nya virusvarianter och bättre behandling.
- Infektion hos den gravida kvinnan
Den omställning av immunförsvaret som sker hos den gravida kvinnan för att inte fostret ska stötas bort kan samtidigt leda till att hon blir sämre ställd vid virusinfektioner, vilket är känt från tidigare influensaepidemier.
Mot bakgrund av sparsamt dokumenterad erfarenhet vid SARS- och MERS-CoV epidemierna med mycket allvarlig sjukdom - graviditetskomplikationer och hög mortalitet - befarade man att gravida skulle vara extra sårbara även vid covid-19. Hos den gravida kvinnan ökar O2 behovet. Att hon då kan svikta vid en sjukdom som engagerar andningskapaciteten är logiskt.
Allteftersom pandemin fortskrider har ett allt större antal gravida kvinnor med SARS-CoV-2 infektion observerats och rapporterats, vilket ökat kunskapen om infektionens förlopp och påföljder hos gravida kvinnor.
Beroende på dynamiken i pandemin har man lanserat ett arbetssätt med kontinuerlig rörlig review av den samlade litteraturen granskad enligt strikta kvalitetskriterier. Den första rapporten publicerades i september 2020 (Allotey et al BMJ) uppdaterades 2 febr 2021 och omfattar nu 192 studier på ca 67.271 SARS-CoV-2 drabbade kvinnor publicerade fram till 6 okt 2020 Läs här
Majoriteten av tidiga studier omfattade vanligen gravida med symtomatisk SARS-CoV-2 infektion och gav översikt av det kliniska förloppet och svår sjukdom.
En bättre bild av risken vid SARS-CoV-2 infektion hos den gravida kvinnan får man i studier baserade på systematisk allmän provtagning och uppföljning av gravida kvinnor som söker vård för symtomatisk sjukdom eller kommer till förlossning. Antikroppsstudier, som behövs för att spåra asymtomatisk/okarakteristisk infektion tidigare under graviditeten, saknas ännu.
Rapporter från nationella register över gravida kvinnor och deras nyfödda baserade på systematisk provtagning för SARS-CoV-2 infektion blir nu successivt tillgängliga från bl a Sverige, Spanien, Italien, UK, USA SARS-CoV-2 (> 50 000 SARS-2 infekterade gravida). Denna typ av studier där hela den gravida populationen studeras under pandemin är av stort intresse eftersom man här kan värdera överrisk över tid och jämföra med icke pandemiska tidsperioder.
Den bild som framträder på nuvarande kunskapsnivå visar att
- risken att bli infekterad verkar vara den samma för gravida och icke gravida
- den största andelen gravida kvinnor (50-80 %) får inte symtom eller bara lindrig sjukdom.
- symtomen är i stort sett samma som hos icke gravida men bl a feber och muskelvärk anges förekomma mer sällan hos gravida.
- merparten gravida kvinnor med covid -19 med lätta - medelsvåra symtom får sällan infektionsrelaterade problem och kan följas och förlösas enligt vanliga obstetriska riktlinjer
- inga data talar för att covid-19 påverkar tidig graviditet/fosterutveckling men fler studier behövs liksom långtidsuppföljning-
- SARS-CoV-2 infektion kan orsaka svår sjukdom hos den gravida kvinnan under andra - tredje trimestern - postpartum, mest frekvent från sen andra och tredje trimestern
- andelen svår sjukdom varierar i olika studier beroende på patienturval och ingående population
- störst risk för svår sjukdom föreligger hos kvinnor med underliggande riskfaktorer: BMI >30, ålder >35 år, hjärtkärlsjukdom, hypertoni, diabetes I och II, kronisk lung–njursjukdom
- etniskt ursprung/socio-ekonomiska förhållanden influerar risken för svår covid-19 vilket framgår särskilt tydligt i registerstudier från UK och USA
- det är viktigt att kritiskt sjuka gravida med andnöd och sviktande vitalfunktioner snabbt tas om hand på ett adekvat sätt - ytterst avancerad intensivvård kan krävas
- en till synes lindrigt sjuk gravid kvinna kan få svåra sjukdomssymtom och behov av snabbt omhändertagande.
- vid svår covid-19 och hypoxi trots syrgasbehandling rekommenderas att man förlöser patienten om det är möjligt
- en central del av patofysiologin vid svår covid-19 infektion är relaterad till en ökad risk för trombo-embolisk sjukdom. Flera begränsade studier rapporterar en hög frekvens av tromboser (30%). Därför är effektiv och tidig antitrombotisk terapi väsentlig och profylax viktigt vid symtomgivande sjukdom, extra viktigt vid samtidig förekomst av riskfaktorer. SFOG råd om hemostasutredning och behandling av venös tromboembolism (VTE), samt trombosprofylax vid Covid-19 hos sjukhusvårdade obstetriska patienter kan läsas här.
- gravida under senare delen av graviditeten har jämfört med icke gravida kvinnor i samma ålder en ökad risk för svår sjukdom med behov av intensivvård och mekanisk ventilation. Det framgår såväl av litteratursammanställningen som den mycket stora registerstudien från CDC i USA som jämför förloppet vid symtomatisk sjukdom hos 23 434 SARS-CoV-2 infekterade gravida och 386 000 inte gravida i samma åldersgrupp (15 - 44 år).
- ett flertal studier anger ökad risk för prematuritet samt viss riskökning för preeklampsi
Orsaken till att gravida oftare skulle kräva intensivvård är oklar men kan svara mot en ökad fysiologisk känslighet vid graviditet. Det är viktigt att notera att mortalitetsrisken för kvinnan med tillgång till adekvat sjukvård fortfarande är mycket låg.Se svenska erfarenheter nedan.
Prematuritets- och sectio-frekvens pga covid -19 var i de tidiga kinesiska rapporterna mycket hög – initialt var rekommendationen i Kina att förlösa alla covid-19 sjuka med sectio. Även i Europa var sectiofrekvensen hög ex vis i Spanien. I registerstudien från UK anges sectio pga covid-19 till 11 % och prematuritetsfrekvensen över 20%.
När det nu är klart att vaginal förlossning inte medför ökad risk för smittöverföring har sectioindikation pga Covid-19 reducerats till kritisk sjukdom hos modern/fosterpåverkan.
Internationella metaanalyser som exempelvis Allotey et al. från BMJ visar ökad risk för allvarlig sjukdom hos modern jämfört med icke gravida. Risk för barnen är också ökad framför allt för prematuritet och neonatalvård . .
I den svenska studien i BJOG av univerisellt testade gravidae, dvs alla testas inför partus, har barnen till test positiva mödrar en ökad risk för neonatalvård med justerad oddskvot 2.24 (95% CI 1.62-3.11). Man ser också en ökad risk för medically indicated preterm birth, dvs förtidig förlossning där man startat förlossningen i förtid, med justerad oddskvot 2.70 (1.60-4.58). Risksiffrorna var högre för de perioder där sjukhus nyttjade selektiv testning.
Test-policy liksom egenskaper hos cirkulerande virusstammar påverkar resultaten i olika studier. Man har från flera håll rapporterat en fortsatt mer än fördubblad risk för neonatalvård och förtidig förlossning hos test-positiva mödrar jämfört med mödrar som inte är testpositiva.
Mortaliteten hos covid-19 infekterade gravida är vid tillgång till adekvat avancerad sjukvård mycket låg men enstaka dödsfall förekommer även här. I länder med otillräcklig sjukvård är situationen svårare och betydligt högre dödstal rapporteras ex vis från Brasilien, Indien.
Det är här viktigt att i varje fall analysera SARS-CoV-2 infektionens roll och även beakta att mödradödlighet vid covid-19 infektion inte alltid behöver vara associerad med de typiska lungsymtomen utan sannolikt även kan vara associerad med andra orsaker som t ex trombosrelaterade komplikationer. Det är inte säkert att covid-19 identifieras i dessa fall utan pandemins effekter på mödradödlighet kan sannolikt bara studeras genom att värdera överrisken i efterhand. Inte minst gäller det vid begränsade sjukvårdsresurser där brist på intensivvårdsplatser kan leda till att allvarliga maternella graviditetskomplikationer inte omhändertages på ett adekvat sätt.
Flera länder har rapporterar att pandemin påverkat kvinnors beteende att söka sjukvård och att detta kan ha negativa effekter för gravida kvinnor med komplicerade graviditeter. Påtvingad lockdown kan också leda till psykiska problem hos den gravida inte minst genom exempelvis svårigheter med försörjning och ökat nära våld.Placenta
Placenta uppvisar inte någon för covid-19 karakteristisk bild, Det finns en stor variation av olika patologiska förändringar av varierande grad och ett spektrum av maternal och fetal vaskulär malperfusion, akut och kronisk inflammation, tromboser i samma utsträcknig som i placentmaterial från icke SARS-CoV-2 infekterade gravidae. Däremot är fibrinavlagringar perivillöst ett karakteristiskt fynd. Mängden inlagring är inte korrelerad till svårighetsgraden av den gravidas covid-19 sjukdom utan återfinns såväl vid asymtomatisk som symtomatisk infektion, Överföring av virus förefaller ovanlig så länge villi trofoblasterna är intakta.
Under senare delen av pandemin har fallrapporter/korta serier kommit om intrauterin/perinatal död i efterförloppet till covid -19 infektion hos ovaccinerade gravida i (slutet av andra-) tredje trimestern utan att modern var svårt sjuk. Virusvarianter var alfa, delta ännu har inga fall orsakade av omicron dykt upp. Sammanställning av 68 kända fall visar karakteristiska placentafynd: - perivillösa - oftast massiva - fibrininlagringar, villi trofoblastnekros med positivt virusfynd och kronisk histiocytär villosit - förändringar som omfattar en stor del av placenta (genomsnittligen cirka ¾). Det leder till svår malperfusion och placentainsufficiens, fosterasfyxi och i de flesta beskrivna fallen fosterdöd. SARS-CoV-2 har överförts till fostret/barnet men infektionen förefaller inte bidra till det svåra förloppet - det är grava hypoxi/asfyxiskador som dominerar obduktionsfynd.
Totalt 13 fall/14 barn) har identifierats i Sverige under en 16 månaders period (se ref Zaigham M et al - detaljerad fallbeskrivning här). Minskande fosterrörelser förde modern till vården i genomsnitt 6 (3-12) dagar efter insjuknandet. 9 barn (ett tvillingpar) föddes levande genom akut sectio pga tecken på svår fosterasfyxi. Två av dem dog perinatalt. Övriga fem dog intrauterint som upptäcktes 2-25 (median 11) dagar efter moderns insjuknande.
Alla dessa gravida var ovaccinerade mot Covid-19.
Vid SARS-CoV-2 infektion hos gravida återtfinns en stor variation av patologiska förändringar - fibrininlagringar och ett spektrum av maternal vaskulär malperfusion, förändringar som kan ses vid svår intrauterin tillväxthämning och preeklampsi.
Eftersom vi känner till att denna placentära fenotyp - kan vara associerad med kardiovaskulära långtidseffekter på barnen är det viktigt att information avseende placenta konsekvent samlas genom placenta undersökning vid misstänkt placentapåverkan av covid-19, Denna information kan komma att visa sig vara väsentlig när långtidseffekter på barnen kommer att utvärderas. - risken att bli infekterad verkar vara den samma för gravida och icke gravida
- Infektion hos fostret och det nyfödda barnet
Det finns endast sparsamma uppgifter om covid-19 i tidig graviditet. Inga hittillsvarande observationer talar för teratogen effekt av SARS-CoV-2. En studie av virusreceptorn ACE-2 i fetal vävnad från 5 normala foster (15 - 38 veckors graviditet) talar i samma riktning: receptorn påvisades inte i hjärnependym – parenkym under hela tidsspannet,
Det finns inte heller rapporterad ökning av spontanabort i anslutning till maternell symtomatisk infektion under första och början av andra trimestern (en enda rapport från gravvecka 19). Däremot leder svår covid-19 sjukdom hos modern i slutet av andra och tredje trimestern ofta till prematur (ofta iatrogen) födsel med ökat behov av neonatalvård. Infektionen förs som regel inte över.
Ökad dödföddhet har inte tidigare observerats. Men under andra (alfa) och tredje smittvågen (delta) rapporteras en viss ökning av covid-19 associerad dödföddhet/perinatal död i nationella studier från USA, England, Skottland, Spanien, Indien. I USA studien var riskökningen högre perioden då virusvarianten delta dominerade än tidigare.
Samtidigt beskrivs en inte tidigare iakttagen virusorsakad höggradig placentit med massiva massiva fibrininlagringar, trofoblastnekros som resulterat i placentadysfunktion/fosterdöd. Virusinfektionen överfördes i majoriteten av fallen. Infekterande virusvarianter tillhörde alfa eller delta. Inga fall har hittills rapporterats från omicron perioden. Den gravida var vanligen inte svårt sjuk eller tom ovetande om covid-19 infektion. Samtliga kvinnor var ovaccinerade (undantagandes en kvinna som just fått sin första dos).
Dessa fall är emellertid sällsynta och kan knappast inverka på statistiken. Risksiffrorna för dödföddhet påverkas förutom av covidinfektionens svårighetsgrad även av många andra faktorer, t ex av virusvariantens smittsamhet och en skev fördelning av vaccinationsgrad i olika befolkningsgrupper. I studierna från England - Skottland framgår god skyddseffekt av vaccination. Nya mer smittsamma virusvarianter sprids mest effektivt i befolkningsgrupper med låg vaccinationstäckning - ofta kopplat med samtidig hög risk för graviditetskomplikationer. I den stora USA registerstudien från CDC angavs inte vaccinationsstatus däremot risk för fosterdöd i olika befolkningsgrupper - lägre risksiffror noteras i regioner där vaccinationsgraden med stor sannolikhet var högre,
I nationella sammanställningar från Sverige och övriga nordiska grannländer ses inte någon statistisk säkerställd ökning av dödföddhet.
Även här har fåtal fall av ovan beskrivna placentadysfunktion/fosterdöd identifierats 3 - 12 dagar efter lindrig maternal covid -19 infektion. Virusvarianten var alfa, som överfördes till alla de fem döda barnen. Alla kvinnorna var ovaccinerade (jmfr ovan den gravida kvinnan/placenta eller läs här).
Det står klart att överföring av smitta till barnet är ovanlig såväl vertikalt som perinatalt.
Från Sverige visar samkörning mellan graviditetsregistret, neonatalregistret och smittskyddsregistret på SARS-CoV-2 RNA fynd hos 0,9% av nyfödda barnen till mödrar som testats positivt under graviditet. Om man begränsade urvalet till kvinnor med positivt test vid förlossningen var 2,7% av deras barn positiva. Den exakta andelen är svår att ange eftersom diagnostiken inte är enhetlig eller optimal och kontaminationsrisk vid provtagningen påtaglig (se nedan avsnitt överföringsrisk och diagnos av fostrets/barnets infektion). I andra vågskålen ligger att flera gravida utan eller med lindriga symtom inte provtagits och därmed inte heller deras barn.
De flesta av de SARS-CoV-2 PCR positiva barnen har befunnits vara och förbli symtomfria men 12 - 20 % har beskrivits ha ofta milda, övergående - covid-19 relaterade symtom: feber, luftvägssymtom, kräkningar, apné, irritabilitet och mycket sällan allvarligare neurologiska symtom. Det är svårt att skilja dessa rapporterade symtom från andra tillstånd relaterade till nyföddhet och prematuritet. Den svenska registerstudien visade att endast 21 barn av 2323 födda av covidpositiva kvinnor hade positiv PCR för SARS-CoV-2. Av dessa var 12 helt friska, 9 hade diagnoser utan klar koppling till covid-19 och inget hade medfödd pneumoni.
Prematuritet, inte infektion, orsakar största behovet av neonatalvård. Barn till covid-19 positiva kvinnor är inte sjukare än andra barn med samma graviditetslängd. Inga dödsfall anges bero på SARS-CoV-2 infektionen hos barnet.
Långtidsuppföljning av barn pågår.
- Överföringsrisk
Smittöverföring från modern kan tänkas ske intrauterint, vid förlossningen, postnatalt genom kontakt-droppsmitta eller amning.
Intrauterin smitta förefaller vara ovanlig men förekommer att döma av fallrapporter/korta serier vid covid-19 hos modern främst vid infektion i tredje trimestern (viremi hos barnet/SARS-CoV-2 fynd i placenta/inre organ vid obduktion). Se WHO Definition and categorization of the timing of mother-to-child transmission of SARS-CoV-2 här
Neonatala Covid-19 positiva nasofarynxfynd neonatalt rapporteras nästan uteslutande bland barn vars mödrar är infekterade vid eller kort tid före partus. I den svenska registerstudien var 17/21 av mödrarna SARS-CoV-2 positiva vid partus.
Liknande data finns I en registerstudie från USA: man fann SARS-CoV- 2 RNA i nasofarynx hos 1,5 % av barnen till >2 800 mödrar med symtomatisk eller asymtomatisk infektion. Alla virusfynd fanns hos barn till mödrar med infektion (positivt PCR test) inom två veckor - majoriteten inom en vecka före partus till 3 dagar efter. Orsak till denna tidsbegränsning kan vara att modern med tidigare infektion inte längre var smittsam vid partus; passivt överförd maternal antikroppsaktivitet kan också spela in. De flesta PCR positiva barn var och förblev asymtomatiska, några hade postnatala symtom inom 5 -7 dagar.
Serologisk kartläggning, nödvändig för att spåra eventuell överföringsrisk under tidigare perioder av graviditeten finns ännu inte. Enstaka fallbeskrivningar finns men det svenska materialet liksom andra material visar att infektion hos modern tidigare under graviditeten kan medföra en något ökad risk för prematuritet men annars ingen negativ inverkan neonatalt hos barnen.
Det serologiska svaret på en covid-infektion eller vaccination hos den gravida kvinnan är studerat och visar samma IgM/IgA/IgG svar mot SARS-CoV-2 spike protein och neutraliserande antikroppar som hos den inte gravida, med en högsta nivå inom 15-30 dagar.
Endast maternal IgG aktivitet förs över transplacentärt till barnet, mer effektivt ju längre intervallet är mellan moderns insjuknande och partus (upp till mer än en månad). Fler studier är angelägna inte bara för att bedöma eventuell tidig överföringrisk utan också för att ta reda på hur länge passivt skydd för det späda barnet varar och för optimering av tidpunkt för vaccination av modern för att åstadkomma bästa skydd för både mor och barn. En nu aktuell studie visar ett cirka 60 % skydd mot sjukhuskrävande covid-infektion under de första 6 månaderna hos barn till mödrar vaccinerade med 2 doser under graviditeten. Omicron varianten var dominerade under studietiden. Studien var inte tillräcklig för att avgöra optimal tidpunkt för vaccination.
Smitta vid förlossningen / postnatalt / amning
Det är det visat att överföringsfrekvensen är oberoende av
- förlossningssätt
- tidig eller sen avnavling
- hud- mot hudkontakt med modern
- rooming in med smittskyddande hygienåtgärder
- amning eller flaskuppfödning
Pasteurisering avdödar virus, donatormjölk säker.
Virus kan finnas i bröstmjölk i akutskedet av infektionen. Neutraliserande IgA antikroppar uppträder tidigt (cirka 5 - 7 dagar) efter infektionen såväl i blod som i bröstmjölk. Barn skulle kunna tänkas bli smittade av bröstmjölk vid en postnatal infektion hos modern under detta tidiga tidsintervall. Presymtomatisk virusutsöndring hos modern har då redan exponerat barnet varför det är av tveksamt värde att störa amningen om moderns tillstånd inte kräver det.
Mycket omfattande erfarenhet visar nu att detta inte är något problem se bl a den svenska barnutfallsstudien.
Personer i omgivningen kan smitta barnet. Infektionen förefaller ofta ha samma vanligen godartade förlopp som efter smitta överförd från modern.
- Laboratoriemetoder
En säker covid-19 diagnos bygger på virologisk diagnostik.
I nuläget bygger rutindiagnostik i- akutfasen på påvisning av virus i form av nukleinsyra alternativt antigen
- konvalescensfasen på påvisning av virusspecifikt antikroppsvar
Diagnostik av covid-19 Schematisk beskrivning, påvisning under infektionsförloppet
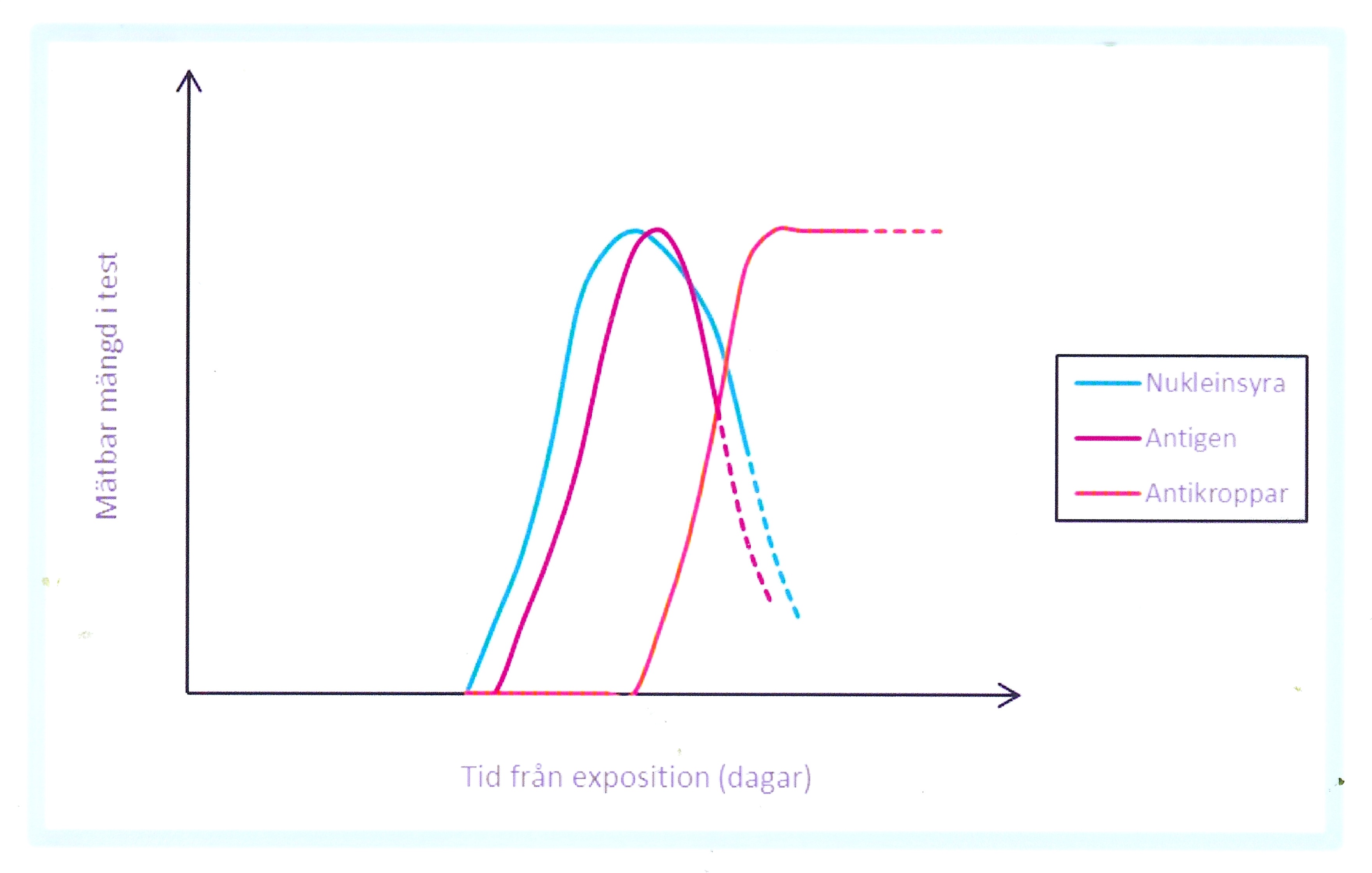
Laboratoriediagnostiken har byggts ut kraftigt för att med diagnostistik och smittspårning begränsa pandemin. Stora satsningar världen över har resulterat i ett utbud av tester av varierande kvalitet i mycket snabb takt.
Tester för diagnos i akutstadiet av infektioner baseras på att påvisa
- virusnukleinsyra med PCR teknik
- fördel hög känslighet och specificitet,
- mängden virus i provet kan anges
- nackdel kräver avancerad utrustning och tränad personal.
- logistikberoende - medför tidsfördröjning
- snabbare tester som förkortar analystiden kommer successivt
- antigentest - påvisar virus höljeproteiner med immunologisk teknik.
- kan utformas som snabbtest med svar inom 10-30 min med de stora fördelar som detta medför
- känsligheten lägre än virusnukleintester -
- i vissa situationer en nackdel (SARS-CoV-2 infekterade individer missas särskilt milda-subkliniska infektioner - kompletterande PCR analys kan behövas)
-i några andra möjligen en fördel - i senförloppet av en SARS-CoV-2 infektion där nukleinsyretester kan vara alltför känsliga och inte speglar smittsamhet
På de etablerade mikrobiologiska laboratorierna utförs fortlöpande kvalitetskontroll för att nå högsta möjliga tillförlitlighet i analyserna. Deras kapacitet täcker sjukvårdens behov men trots uppskalning och kompletterande laboratorier är det svårt att täcka det totala behovet
Snabbtester, även självtester är i den rådande pandemisituation ett komplement och verktyg för smittspårning i öppen vård. Specificitetskraven måste vara höga > 99,5 %!
FoHM:s Vägledning för användning av antigentester vid covid-19 läs här och instruktioner om hur testerna kan användas och tolkas här .
PCR-diagnostik
Mycket känsliga RT-PCR tester används för diagnos vid akut sjukdom.Virus-RNA kan påvisas under akutskedet av sjukdomen under cirka 5-9 dagar - hos svårt sjuka ännu längre och ofta i mycket höga koncentrationer.
En mängd provmaterial kan användas. Nasofarynx/svalg-salivprov vanligast där vältaget nasofarynxprov ger säkrast resultat.
Provkvalitet av stor vikt för utfallet. Beakta vid provtagningen alltid risken för kontamination från omgivningen eftersom testmetoden är mycket känslig.
- Falsk negativt RT-PCR resultat kan ses mycket tidigt i infektionsförloppet. Vid covid-19 misstänkt sjukdom bör nytt prov tas om annan diagnos inte erhållits.
- Under sjukdomens senare fas med svårt nedre luftvägsangrepp kan nasofarynx/orofarynx prov vara negativt samtidigt som stora mängder virus återfinns i bronkialsekret/bronkoalveolärt lavage.
- Pos RT-PCR-resultat anger endast närvaro av virus RNA och virus oavsett om det är infektiöst eller bundet till antikropp och inte längre infektiöst. Ett positivt resultat är därför inte säkert liktydigt med smittsamhet.
- När stora mängder nukleinsyra påvisas är det mycket sannolikt att det rör sig om smittsam patient.
- Vid mycket låg aktivitet kan förnyat prov behövas för att utesluta kontamination vid provtagning respektive tidig fas av SARS-CoV-2 infektion.
- Ett kvantitativt mått kan också vara av värde i behandlingssituationer; laboratorier kan ange ett s k Ct (cycle threshold) värde dvs antal reaktionscykler då reaktion upptäcks:
ett lågt Ct värde avspeglar tidigare upptäckt virus = högre mängd
ett högre Ct värde motsvarar alltså en lägre mängd
Observera dock att jämförelse mellan olika Ct värden endast kan göras mellan värden erhållna med samma analysmetod. Tyvärr är standardisering mellan olika tester ännu inte åstadkommen.
Antigendiagnostik
är inte lika känsligt som RT-PCR.
Om antigentester används för att ställa covid-19 diagnos rekommenderar Folkhälsomyndigheten att testet tas vid symtom och senast dag fem i infektionsförloppet läs här.Påvisning av infektiöst virus genom virusisolering i vävnadskultur är bästa måttet på smittsamhet. Tekniken kräver säkerhetslaboratorium och är för tids- och arbetskrävande för rutinbruk. Används vid speciella frågeställningar.
Serologiska analyser
Översikt från FoHM Serologisk test - vägledning för antikroppspåvisning läs här
IgG tester
Indikation för analys är- misstänkt infektion trots att RT-PCR utfallit negativ
- man söker markör för misstänkt tidigare genomgången infektion
Man kan påvisa virusspecifika IgG antikroppar efter någon vecka till en dryg månad efter infektionsdebut.
Prov för antikroppsanalys bör man inte ta förrän minst 2 veckor efter tillfriskande.
Ett positivt svar hos en ovaccinerad individ visar genomgången infektion eller pågående långdragen covid-19 infektion.
Med hjälp av tester, som har bra prestanda finner man antikroppar hos SARS-CoV-2 infekterade med enstaka undantag.
Men antikroppssvaret kan i synnerhet hos patienter med mild infektion vara låg och inte mätbart i alla rutintester på marknaden.Högsta möjliga specificitet och sensitivitet krävs för rättvisande resultat. Speciellt viktigt för serologisk screening av SARS-CoV-2 spridning i befolkningsgrupper.
Ett positivt IgG-antikroppssvar hos en ovaccinerad individ kan vara av värde för påvisa genomgången infektion främst vid medicinska frågeställningar.
Baserat på den kunskap vi har idag, bedömer Folkhälsomyndigheten att ett positivt antikroppssvar i likhet med ett positivt RT-PCR-svar eller ett positivt antigensvar indikerar skydd mot återinfektion med allvarliga symtom 5-6 månader från infektionstillfället (FoHM:s vägledning för bedömning av immunitet läs här).
Neutralisationstest mäter antikroppar kan vara bättre korrelerade till skydd än de rutinmässigt använda antikroppstesterna och kan dessutom fylla behovet av verifikationstest. Traditionella Nt-tester är arbetskrävande och måste utföras på säkerhetslaboratorium.
I en tidig studie från Göteborg påvisades neutraliserande antikroppar hos alla 49 patienter såväl med lindrig som svår sjukdom – även 3 patienter utan antikroppsaktivitet i känsliga rutinmetoder. Används speciellt för att i laboratoriet förutse olika vacciners skyddseffekt mot nya virusvarianter.
Nya tekniker har utarbetats för att mäta samma funktionella antikroppar utan användning av infektiöst virus.
IgM-tester
Används inte för rutindiagnostik av aktuell infektion.
Indikationer för provtagning är för närvarande serologisk diagnos av kongenital eller tidig neonatal covid-19 infektion hos det späda barnet.Maternal IgM-aktivitet passerar inte placenta och sådan aktivitet är alltså barnets egenproduktion.
Virusspecifika IgG aktivitet hos det späda barnet domineras av transplacentärt överförd maternal IgG antikroppsaktivitet.
Det betyder alltså bara att modern haft covid-19.
Saknas sådan aktivitet har modern inte haft infektionen om det inte varit så sent att modern inte hunnit bilda antikroppar.
IgA - tester
IgA aktivitet kommer i blodet och bröstmjölk nästan lika snabbt i sjukdomsförloppet som IgM. Förs inte över placenta från mor till barn.Används vid speciella frågeställningar.
Uppföljning av virusmutationer
SARS-CoV-2 stammar insamlade över tid och olika delar av världen följs med sekvensering av hela virusgenomet för att upptäcka mutationer av betydelse för virulens och immunitet (se vidare FoHM här och helgenomsekvensering här).Samma teknik kan också användas för att spåra smittvägar.
För att något enklare följa spridning av virus med redan kända mutationer används PCR metoder selektivt riktade mot avvikande delar av genomet. Nya mutationer kan då inte upptäckas - för det krävs sekvensering av hela genomet.
I patientdiagnostiken används däremot tester som samtidigt spårar flera olika delar av SARS-CoV-2 genom för att undvika falskt negativa resultat vid infektion med eventuella nya mutationer.
- akutfasen på påvisning av virus i form av nukleinsyra alternativt antigen
- Diagnos av moderns infektion
Symtom misstänkta för covid-19, se nedan avsnitt 12.
Nasofarynx/orofarynx sekret, sputum, bronkialsekret, bronklavage kan användas för analys med RT-PCR SARS-CoV-2.
- Andra kroppsvätskor som t.ex. serum, blod, amnionvätska, bröstmjölk, urin, vaginalsekret kan tas vid speciella frågeställningar.
- Serologisk undersökning för diagnostik tas alltid om barnet utreds för prenatal smitta (se nedan)
Utvecklingen av analys- och provtagningsmetoder är snabb - håll kontakt med anlitat laboratorium.
- Andra kroppsvätskor som t.ex. serum, blod, amnionvätska, bröstmjölk, urin, vaginalsekret kan tas vid speciella frågeställningar.
- Undersökning av placenta
Omhändertagande av placenta
Det är önskvärt att placenta analyseras avseende eventuell påverkan vid SARS-CoV-2 infektion. Placenta skickas till avdelningen för patologi för placenta PAD samt analys av SARS-CoV-2 - se laboratoriets föreskrifter.
Se också WHO Definition and categorization of the timing of mother-to-child transmission of SARS-CoV-2 här - Diagnos av fostrets/barnets infektion
Rutinmässig provtagning på barn till kvinnor med positiv test för SARS-CoV-2 behöver inte utföras.
Vid inläggning på neonatalavdelning:
Nasofarynx/orofarynx prov för RT- PCR vid 2, 4 och 7 dygns ålder.
Har modern hög feber, sepsisliknande sjukdomsbild
eller
är i behov av intensivvård
tas även PCR-prov från barnets blod så snart som möjligt.
Vid provtagning: tänk på att virus ofta finns i omgivningen och att PCR analysen har mycket hög känslighet.Se vidare handläggning nedan.
- Profylax
Hittills har Folkhälsomyndigheten rekommenderat vaccin till alla gravida för att minska risken för svår sjukdom. From hösten 2025 är denna rekommendation borttagen men gravida med tillstånd/läkemedel som påverkar immunförsvaret negativt samt gravida med svår lungsjukdom tex cystisk fibros rekommenderas även fortsättningsvis vaccin mot covid-19.
2022-06-03 sammanfattar Svenska Barnmorskeförbundet, SFOG och NPO Kvinnosjukdomar och förlossning dokumenterad erfarenhet av covid-19 vaccination under graviditet: data från nordiska och internationella studier visar att vaccination mot covid-19 är säkert under graviditet och vaccinet skyddar mot svår infektion och dess komplikationer hos mor och barn. Vaccination ger ett gott skydd mot allvarlig sjukdom och gravida kvinnor bör därmed kunna genomföra arbetsuppgifter även där viss risk för exposition av viruset kan finnas. Läs hela texten härSe även information från Folkhälsomyndigheten här och från Arbetsmiljöverket här.
Stora uppföljningsstudier av vaccination av 157 521gravida i Sverige/Norge (läs här) (huvudsakligen med mRNA vaccin) liksom sammanställning av internationella data för >117 000 vaccinerade gravida (läs här) och europeiska smittskyddsinstitutet EMA:s granskning av data för 65 000 vaccinerade gravida och deras barn (läs här) bekräftar säkerheten t ex ingen ökad risk för graviditetskomplikationer, missfall, för tidig födsel eller negativa effekter på de ofödda barnen oavsett när under graviditeten vaccinet getts.Intervall mellan covid-19 vaccination och anti-D profylax
Folkhälsomyndigheten rekommenderar minst 7 dagar. Någon interaktion är inte att förvänta, rekommendation görs för att hålla isär ev. biverkningar
Covid-19 vaccination och influensavaccination:Vaccin mot covid-19 och standarddos influensavaccin kan ges vid samma tillfälle (olika injektionsställen ska användas).
Covid-19 vaccination och RSV vaccin.
Det rekommenderas att covid-19-vaccin och vacciner som nyligen blivit godkända - t ex RSV-vaccin - inte ska ges samtidigt med Covid-19.
Intervall mellan covid-19 vaccination och MMR och andra vaccin:ska enligt FoHM vara minst 7 dagar.
- Terapi
Vid mild sjukdom rekommenderas att patienten isolerar sig i hemmet med symtomatisk behandling.
Patienter som sjukhusvårdas med måttlig till allvarlig sjukdom får behandling med syrgas och intensivvård vid behov. Erfarenheterna av behandling och omhändertagande inom sjukvården, och speciellt inom intensivvården, har sedan våren 2020 inneburit minskad mortalitet av patienter med covid-19.
Se rekommendationer i Nationellt vårdprogram för covid-19 läs här
Samtidig bakteriell infektion är ovanlig vid covid-19 varför antibiotikabehandling sällan är indicerat initialt.
Antikoagulantia
Pga den kraftigt ökade risken för tromboemboliska komplikationer får alla patienter som sjukhusvårdas trombosprofylax under sjukhusvistelsen och en tid därefter. Trombosprofylax kan övervägas även hos icke - sjukhusvårdade. SFOG har utarbetat råd om behandling av venös tromboembolism (VTE), samt trombosprofylax vid covid-19 hos sjukhusvårdade obstetriska patienter och kan läsas här
Antiviral terapi
Remdesivir, ett antiviralt läkemedel, är registrerat och godkänt av EMA och Läkemedelsverket för behandling av Covid.19 hos patienter över 12 år. Effekten av remdesivir bedöms som måttlig. Klinisk effekt har dock påvisats vid tidig behandling av en tydligt definierad subgrupp med sannolikt hög virusreplikation. Ingen effekt vid senare svår sjukdom.
Remdesivir kan därför övervägas tidigt i förloppet (≤ 7 dagar) till sjukhusvårdade patienter i försämringsfas med hypoxi och behov av syrgasbehandling. Remdesevir är även godkänt av EMA för tidig behandling av patient med risk för svår sjukdom. Kontraindikationer såsom njurfunktionsnedsättning eller leversvikt skall beaktas.
Remdesivir har givits även till gravida utan negativa effekter även om erfarenheten är begränsad.
Remdesivir ges som intravenös infusion (200 mgx1 iv dag 1, sedan 100 mg iv dagligen). Behandlingen bör avslutas efter 5 dagar.
Monoklonala antikropparAntivirala monoklonala antikroppar har i flera studier visats kunna hindra sjukdomsutveckling hos immunsupprimerade. Dessa preparat är godkända för behandling av mild till måttlig covid-19 hos vuxna och barn över 12 år som har hög risk för svår covid-19, exempelvis personer med nedsatt immunförsvar. Kan ges till gravida.
Effekten av denna grupp läkemedel är i varierande grad känslig för mutationer i spikegenomet och därför beroende av egenskaper hos infekterande virusvariant. För närvarande dominerar tyvärr varianter med neutralisationsresistens mot alla tillgängliga monoklonal preparat varför behandling eller pre - expositionsprofylax med monoklonala antikroppar inte rekommenderas. I enskilda angelägna fall kan analys av aktuell virusvariant göras för att bedöma virusvariant i förhållande till neutralisationskänslighet för tillgängliga monoklonaI preparat. Aktuella preparat se Läkemedelsverket, aktuell virusvariant se FHM. Se vidare nationellavårdprogram mot Covid-19 här.Kortikosteroider
Lågdos dexamethason godkänt av EMA/Läkemedelsverket har visats reducera mortaliteten med en tredjedel hos respiratorvårdade patienter och med 1/5 hos patienter med enbart syrgasbehov. Därför erbjuds dexamethason/betametason - 6 mg x 1 dexametason (alternativt betametason 5–6 mg x 1) p.o eller i.v. i upp till 10 dagar - till sjukhusvårdade patienter med ihållande syrgasbehov och inflammationstecken (feber, CRP-stegring) om mer än 7 dagar har gått sedan symtomdebut. Preparaten anses ha likvärdig effekt.
Kan ges till gravida och ammande.
Övriga preparat
Det finns ingen eller mycket begränsad erfarenhet av behandling av gravida med många läkemedel mot covid-19 t ex paxlovid (nirmatrelvir (PF-07321332)/ritonavir) oral antiviral med visad god effekt. Se vidare artikel från Janus nedan.
Nationellt vårdprogram för covid-19 läs här
Läkemedelsverkets förteckning över
godkända coronamediciner och medel under granskning på EMA läs här.
godkända Covid-19 vaccin och vaccin under granskning på EMA läs härEuropean Medical Agency EMA https://www.ema.europa.eu
Winblad B, Nörby U. 22-05-04.Läkemedel vid covid-19 under graviditet. Janusinfo läs här
Läkemedelsstudier finns registrerade på www.clinicaltrials.gov - Svenska erfarenheter
Undan för undan ökar erfarenheten av gravida med covid-19 i Sverige. Vi bevakar kontinuerligt läget och försöker hålla Infpregs användare uppdaterade.
Stockholm har hittills varit hårdast drabbat av covid-19 pandemin. Systematisk provtagning av 682 kvinnor som fött på Karolinska 25/3 - 27/4 visade 6,6% SARS-CoV-2 RT-PCR positiva - drygt hälften hade inga symtom. Under perioden 28/4 - 24/9 (då Karolinska slutade screena alla gravida inom slutenvården) har antalet PCR-positiva patienter successivt minskat till <0,2 % i augusti/september 2020. Sammantaget har 65 - 70 % av de PCR-positiva kvinnorna varit helt symtomfria.
Även om de flesta covid-19 födande haft inga eller lindriga symtom så ställs extra krav på vården för att minimera smitta till personalen. Besked till den födande om positivt provsvar har också inneburit stor oro hos många.
Gravida, som är så svårt sjuka att intensivvård krävs, följs med extra stor noggrannhet.
I hela landet hade fram till och med 1 oktober 2021 minst 73 gravida krävt IVA vård pga svår covid 19-sjukdom – varav några i ECMO. 67% förlöstes prematurt (jämför genomsnitt normalt 5,3%) 75% förlöstes med sectio (genomsnittligen normalt 18%). Tre fall av maternell död med klar association till svår covid 19-infektion har hittills (1 dec 2021) inträffat vad Infpreg känner till. Enstaka fall av lungemboli hos gravida med covid 19 finns (se fallrapporter).
Inga fullvaccinerade återfinns bland IVA vårdade eller döda.
Flera fall av lindrig maternell sjukdom men uttalad placentapåverkan och fetal asfyxi.
De svenska kvalitetsregistren har föredömligt snabbt ställt om till denna nya verklighet, och ett flertal register har fått tillstånd från etikkommitté att studera graviditets- och barn-utfall vid covid-19.
Utfall hos >2300 barn till mödrar med covid-19 under graviditeten har studerats genom samkörning mellan graviditetsregistret, neonatalregistret och smittskyddsregistret. Rapporterade data - se ovan under 5 eller läs här - visar att pågående SARS-CoV.2 infektion hos de födda barnen är ovanliga, oftast lindriga. Några barn var födda extremt prematurt. I övrigt har inga barn varit svårt sjuka av infektionen. Däremot sågs ökade respiratoriska problem beroende på måttligt ökad prematuritet. Samvård mor barn med amning leder inte till infektionsproblem.
Folkhälsomyndigheten har i samarbete med SFOG sänt underlag till Socialstyrelsen för bedömning och ställningstagande till om åtgärder ska vidtas för att minska smittrisk av gravida. Information från Folkhälsomyndigheten - Gravida med Covid-19 (april 2020)
Genom en matchning mellan SMINET (Folkhälsomyndighetens register som innehåller information om datum för insjuknande i covid-19 eller positivt testresultat), Graviditetsregistret (med information om graviditet, förlossningar, och barnutfall), Svenskt Neonatalregister (SNQ), och Patientregistret (PAR) har Socialstyrelsen den 29 april 2021 tagit fram underlag för en förnyad bedömning av om covid-19 under pågående graviditet innebär en ökad risk för mor eller barn (läs här)
Socialstyrelsens slutsats: Kvinnor som får en covid-19-infektion under graviditetsveckorna 22-36 löper en väsentligt högre risk än andra kvinnor att föda prematurt. Det finns också en statistiskt säkerställd ökad relativ risk för tromboser och/eller koagulationsrubbningar bland gravida kvinnor med covid-19, men den absoluta risken är låg. (läs hela bilagan här)
FoHM har 25 maj 2021 rekommenderat att vaccination erbjuds alla gravida kvinnor (se profylax avsnittet). Anslutningen till vaccinationen är ännu (fram till 1:a december 2021) låg genomsnittligen knappt 50%, lägre än bland jämnåriga icke gravida. Andelen varierar över landet från 44 till 68% .
För att snabbare öka den gemensamma kliniska erfarenheten av de som blir sjuka har vi skapat en modul där de mycket givande användarrapporterna kan läsas. Använd ert eget vanliga INFPREG lösenord.
Nya rapporter är mycket välkomna och lärorika. Skicka in en doc eller pdf fil till infpreg.karolinska@sll.se så lägger vi ut den. Detta är den säkraste lösningen - den tidigare möjligheten att lägga in filen själv är nu inte tillgänglig,
Se vidare svenska erfarenheter överst i referenslistan. - Handläggning
SVENSK FÖRENING FÖR OBSTETRIK OCH GYNEKOLOGI & SVENSKA NEONATALFÖRENINGEN REKOMMENDATION OM HANDLÄGGNING AV GRAVIDA OCH NYFÖDDA BARN TILL KVINNOR MED VERIFIERAD/SANNOLIK COVID-19 Version 4, uppdaterad 2022-02-18 För Svensk förening för obstetrik och gynekologi: Olof Stephansson, Sissel Saltvedt, Karin Pettersson För Svenska neonatalföreningen; Mikael Norman, Erik Normann, Lars Naver
1. ALLMÄNT
• Covid-19 förekommer i samma utsträckning bland gravida kvinnor som i den allmänna befolkningen.
• Inga data talar för att Covid-19 påverkar tidig graviditet/fosterutveckling men fler studier behövs
• SARS-CoV-2 positiva mödrar har ingen signifikant ökad risk för dödföddhet.
• SARS-CoV-2 infektion kan orsaka svår sjukdom hos den gravida kvinnan under andra hälften av graviditeten och postpartum. Det är viktigt att kritiskt sjuka gravida med sviktande vitalfunktioner snabbt tas om hand på ett adekvat sätt - avancerad intensivvård kan krävas.
• Vaccin rekommenderas till alla gravida. Vaccinet kan ges före, under och efter graviditet.
• Läkemedel mot svår sjukdom (antivirala läkemedel, monoklonala antikroppar, steroider) bör inte undanhållas gravida.
• Risken för medicinskt indicerad förtidsbörd ökar hos gravida med svår Covid-19, vilket medför ett ökat behov av neonatalvård för deras barn. Risken för spontan förtidsbörd vid Covid-19 är inte ökad.
• Barn till SARS-CoV-2-positiva kvinnor har inte en ökad risk för sjuklighet jämfört med barn födda med jämförbar graviditetslängd. Om barnet föds tidigt löper det samma risk för komplikationer och framtida funktionshinder som andra tidigt födda barn.
• SARS-CoV-2-positiva mödrar överför sällan viruset till sina barn. Den överföring som sker är till övervägande del postnatal.
• De flesta SARS-CoV-2 positiva barn är symtomfria.
• I Sverige har inga fall av allvarlig sjukdom eller död hos nyfödda som testat positivt för SARSCoV-2 beskrivits där Covid-19 har påvisats vara den direkta orsaken. Andra orsaker har i samtliga fall varit väsentligt mer sannolika.
2. SMITTSAMHET
• Smittöverföring av SARS-CoV-2 mellan mor och barn förekommer i 1% av alla test-positiva mödrar och 3% hos mödrar som testat positivt i anslutning till förlossning. Den kan ske intrauterint eller vid förlossning men den vanligaste vägen är postnatalt genom dropp/kontakt/stänksmitta.
• Inget tyder på att vaginal förlossning medför en ökad risk för smittöverföring jämfört med kejsarsnittsförlossning.
• Virus har påvisats i bröstmjölk men amning är osannolik som smittväg.
• Nyfött barn som inte vistats hos Covid-19-positiv förälder efter födelsen kan betraktas som oinfekterat.
• Nyfött barn som har vistats hos förälder med Covid-19 efter födseln betraktas som misstänkt infekterat, oavsett om barnet har symtom på sjukdom eller inte.
• Inget fall av smitta från ett nyfött barn till omgivningen finns beskrivet.
3. FÖRLOSSNING
• PCR-provtagning för SARS-CoV-2 rekommenderas på alla kvinnor med symtom förenliga med Covid-19.
• Förlossningssätt styrs utifrån sedvanliga obstetriska överväganden.
• Den obstetriska handläggningen antenatalt och intrapartalt sker enligt riktlinjer för icke smittad kvinna. Lustgas kan användas. Skalpelektrod inkl. skalpprovtagning på sedvanliga indikationer. Avnavling enligt klinikens rutin.
• Om patienten har stigande syrgasbehov och inte kan syresätta sig adekvat på 4–5 L O2/min och om graviditetslängden är >28 graviditetsveckor (individuell bedömning vid graviditetslängd <28 veckor) bör man överväga förlossning inom närmaste dygnet. Det postoperativa förloppet är inte sällan komplicerat.
• Vid behov av att inducera fetal lungmognad ges kortison på sedvanligt sätt och man bör beakta att även en singeldos (12 mg Betapred) givet timmar före partus har associerats med signifikant högre överlevnad hos det tidigt födda barnet.
• Magnesiumsulfat ges på sedvanliga indikationer.
• Lågmolekylärt heparin ska ges på vida indikationer under graviditet, i samband med förlossning och postpartum ffa vid slutenvårdskrävande sjukdom.
4. BARN FÖDDA AV KVINNOR MED LUFTVÄGSSYMTOM UTAN ETIOLOGISK DIAGNOS
• Barn till kvinnor med stark misstanke om Covid-19, där svar på test för SARS-CoV-2 inte är klart handläggs i väntan på testresultat på samma sätt som barn till kvinnor med positiv provtagning enligt punkt 5.
5. BARN FÖDDA AV KVINNOR MED POSITIV PROVTAGNING FÖR SARS-COV-2 5.1 OMEDELBAR HANTERING
• Barn och mor vårdas tillsammans om inte neonatal HLR eller neonatalvård förväntas.
• Mor och barn separeras direkt i de fall där barnet behöver HLR och där neonatalvård sannolikt kommer att behövas. Det medger möjlighet att betrakta barnet som initialt smittfritt. 5.2 BARN I BEHOV AV NEONATAL HLR
• Barnet förs direkt ut ur förlossningsrummet, tas emot av personal från neonatalavdelning eller förlossning och förs till barnakutbord på annat rum.
• Barnet kan primärt betraktas som icke smittsamt.
5.3 BARN DÄR MAN DIREKT KAN BEDÖMA ATT DET BEHÖVER NEONATALVÅRD
• Barnet kan primärt betraktas som icke smittsamt.
• Vårdas om möjligt i enkelrum på neonatalavdelning tillsammans med frisk partner eller annan person som föräldrarna utser.
• Covid-19-positiv mor kan efter tillfrisknande komma till neonatalavdelningen enligt Folkhälsomyndighetens riktlinjer för exponerad person.
5.4 BARN SOM BEHÖVER NEONATALVÅRD EFTER ATT HA VISTATS TILLSAMMANS MED SJUK MOR 5.4.1 VÅRDAS I ENKELRUM PÅ NEONATALAVDELNING TILLSAMMANS MED FRISK PARTNER ELLER ANNAN PERSON SOM FÖRÄLDRARNA UTSER.
• Vid behov av andningsstöd transporteras barnet i kuvös från förlossning/BB till neonatalavdelning.
• Barnet betraktas primärt som infekterat.
• Barnets vårdnadshavare får inte lämna enkelrummet och inte vistas i neonatalavdelningens allmänna utrymmen.
5.4.2 SAMVÅRD MED MODERN
• Kan vara ett alternativ om avdelningens utformning och bemanning tillåter om intensivvård inte behövs och om barnet kan vårdas på enkelrum.
• Vid behov av andningsstöd transporteras barnet i kuvös från förlossning/BB till neonatalavdelning.
• Barnet betraktas primärt som infekterat.
• Strikt karantän på rummet. Anhörig som vårdar barnet ska inte vistas i neonatalavdelningens allmänna utrymmen.
5.5 BARN SOM ÄR PÅVISAT INFEKTERADE 5.5.1 VÅRDAS I ISOLERINGSRUM PÅ NEONATALAVDELNING TILLSAMMANS MED FRISK PARTNER ELLER ANNAN PERSON SOM FÖRÄLDRARNA UTSER.
• Barnet transporteras alltid i kuvös till och från isoleringsrummet.
• Föräldrar, partner ska inte lämna rummet och inte vistas i neonatalavdelningens allmänna utrymmen.
5.5.2 SAMVÅRD MED MODERN
• Kan vara ett alternativ om avdelningens utformning och bemanning tillåter om intensivvård inte behövs och om barnet kan vårdas på enkelrum.
• Barnet transporteras alltid i kuvös till och från rummet.
• Strikt karantän på rummet. Anhörig som vårdar barnet ska inte vistas i neonatalavdelningens allmänna utrymmen.
5.6 BARN MED VERIFIERAD/SANNOLIK COVID-19 VID RISK FÖR AEROSOLBILDNING
• Risk för aerosolbildning föreligger vid intubation/extubation, CPAP och respiratorvård. Högflödesgrimma ska undvikas.
• Barnet transporteras i kuvös till och från vårdplats.
• Vårdas i isoleringsrum på neonatalavdelning tillsammans med frisk partner eller annan person som föräldrarna utser.
• Kuvösvård rekommenderas.
• Personskydd: Enligt sjukhusets rutiner vid risk för aerosolbildning.
• Mikrobiologiskt filter på expirationsslangar.
• Slutet sugsystem.
5.7 BARN SOM INITIALT INTE BEHÖVER HLR ELLER NEONATALVÅRD MAMMA SOM FÖRVÄNTAS KUNNA TA HAND OM SITT BARN UNDER HELA VÅRDTIDEN PÅ BB
• Samvård i enkelrum.
• Noggranna hygienrutiner vid skötsel och amning med följande råd till modern:
• Tvätta händerna innan kontakt med barnet, bröstpumpen eller flaskorna.
• Undvik att hosta eller nysa på barnet medan du matar.
• När en bröstpump används, följ rekommendationerna för rengöring av pumpen efter varje användning för att hindra smitta till barnet.
• Barnet betraktas som infekterat.
• Barnläkarundersökning av det nyfödda barnet enligt normala rutiner, extra läkarkontroller endast på medicinsk indikation.
• Hemgång från sjukhuset enligt ordinarie rutiner
6. BARN FÖDDA AV KVINNOR MED POSITIV PROVTAGNING FÖR SARS-COV-2 I BEHOV AV ÅTERINLÄGGNING 6.1 VÅRDAS I ENKELRUM/ISOLERINGSRUM
• Transporteras till neonatalavdelning i kuvös.
• Betraktas som potentiellt smittsamt och provtas.
• Vårdas i enkelrum/isoleringsrum på neonatalavdelning tillsammans med frisk partner eller annan person som föräldrarna utser.
6.2 SAMVÅRD MED MODERN
• Kan vara ett alternativ om avdelningens utformning och bemanning tillåter, om
• intensivvård inte behövs och om mor och barn kan vårdas på enkelrum.
• Transporteras till neonatalavdelning i kuvös.
• Modern ska inte lämna rummet och inte vistas i neonatalavdelningens allmänna utrymmen
7. PROVTAGNING PÅ BARN FÖDDA AV KVINNOR MED POSITIV PROVTAGNING FÖR SARS-COV-2 7.1 PROVTAGNING PÅ BB-BARN
• Rutinmässig provtagning på barn till kvinnor med positiv test för SARS-CoV-2 behöver inte utföras.
7.2 PROVTAGNING VID INLÄGGNING PÅ NEONATALAVDELNING
• Provtagning med PCR NPH vid 2, 4 och 7 dygns ålder.
• Har modern hög feber, sepsisliknande sjukdomsbild eller är i behov av intensivvård tas även PCR-prov från barnets blod så snart som möjligt.
8. UPPFÖLJNING AV BARN FÖDDA AV KVINNOR MED POSITIV PROVTAGNING FÖR SARS-COV-2
• Det är viktigt med sedvanlig neonatal uppföljning inklusive PKU-provtagning.
• Mödrar eller barn som inte friskförklarats från Covid-19 ska hållas isär från andra mottagningspatienter
• Föräldrarna rekommenderas kontakta sjukvården vid tecken på infektion hos barnet.
9. REGISTRERING I JOURNAL OCH KVALITETSREGISTER, SAMT SMITTSKYDDSANMÄLAN
• Vid bekräftat fall (mödrar och barn) i slutenvård ska smittskyddsanmälan göras i SmiNet.
• Covid-19-positiva gravida kvinnor: Diagnoskoden U07.1 ska användas. Det är mycket viktigt att registrera diagnoskoden även i den obstetriska journalen.
• Samtliga barn till SARS-CoV-2-positiva mödrar ska vid barnläkarundersökning diagnoskodas i FV2. De som läggs in för neonatalvård ska också registreras i Neonatalregistret (SNQ).
• Barn utan symtom som inte provtagits eller där provtagning utförs p.g.a. misstanke/vetskap om exponering för smitta och provsvaret inte är klart eller inget virus påvisas kodas med Z20.8.
• Barn med positiv virusdiagnostik för SARS-CoV-2 ska erhålla diagnoskod U07.1 och om barnet har symtom, följt av kod för manifestation (till exempel medfödd viruspneumoni P230). - Referenser
Svenska erfarenheter
Magnus MC, Örtqvist AK, Dahlqwist E et al. Association of SARS-CoV-2 Vaccination During Pregnancy With Pregnancy Outcomes. JAMA. 2022 Mar 24. doi: 10.1001/jama.2022.3271. Epub ahead of print. Läs här
Norman M, Navér L, Söderling J, Ahlberg M, Hervius Askling H, Aronsson B, Byström E, Jonsson J, Sengpiel V, Ludvigsson JF, Håkansson S, Stephansson O. Association of Maternal SARS-CoV-2 Infection in Pregnancy With Neonatal Outcomes. JAMA. 2021 Apr 29. doi: 10.1001/jama.2021.5775. Epub ahead of print. Läs här
Pettersson K, Naver L, Covid-19 hos gravida ofta lindrig - svår sjukdom kan dock uppstå. Sannolikt ingen ökad risk för sjuklighet hos barnet, men risken ökar för förtidsbörd och därmed för komplikationer. Läkartidningen. 2021;118:20217 Läs här
Ahlberg M, Neovius M, Saltvedt S, Söderling J, Pettersson K, Brandkvist C, Stephansson O. Association of SARS-CoV-2 Test Status and Pregnancy Outcomes. JAMA. 2020 Sep 23:e2019124. doi:10.1001/jama.2020.19124 Epub ahead of print. Läs här
Remaeus K, Savchenko J, Brismar Wendel S, Gidlöf SB, Graner S, Jones E, Molin J, Saltvedt S, Wallström T, Pettersson K. Characteristics and short-term obstetric outcomes in a case series of 67 women tested positive for SARS-CoV-2 in Stockholm, Sweden. Acta Obstet Gynecol Scand. 2020 Sep 27:10.1111/aogs.14006. Läs här
Pasternak B, Neovius M, Söderling J et al. Preterm Birth and Stillbirth During the COVID-19 Pandemic in Sweden: A Nationwide Cohort Study. Ann Intern Med. [Epub ahead of print 12 January 2021]. doi:10.7326/M20-6367
Comment Farr A; Falcone V; Wagner M, Medical University of Vienna, Vienna, Austria 5 February 2021
Zaigham M, Tannenberg, P. Intrauterin smitta och akut placentasvikt vid covid-19 hos gravid, Läkartidningen 11-12/2021 Lakartidningen.se 2021-03-05
Andersson E, Sönnerborg A. Framtida testning för sars-cov-2 – inte bara mer utan smartare. Läkartidningen 49-50/2020. Läs här
Rudberg AS, Havervall S, Månberg A, Jernbom Falk A et al. SARS-CoV-2 exposure, symptoms and seroprevalence in healthcare workers in Sweden. Nat Commun. 2020 Oct 8;11(1):5064. doi: 10.1038/s41467-020-18848-0. Läs här
Aktuella referenser om skyddseffekt av vaccination av gravida för mor och barn
Stock SJ, Carruthers J, Calvert C et al. SARS-CoV-2 infection and COVID-19 vaccination rates in pregnant women in Scotland. Nat Med. 2022 Jan 13. doi: 10.1038/s41591-021-01666-2. Epub ahead of print. PMID: 35027756. läs här
Se även Läkemedelsverkets bevakning av vaccination av gravida: Milda och övergående biverkningar även för gravida läs här
Halasa NB, Olson SM, Staat MA. Effectiveness of Maternal Vaccination with mRNA COVID-19 Vaccine During Pregnancy Against COVID-19-Associated Hospitalization in Infants Aged <6 Months - 17 States, July 2021-January 2022. MMWR Morb Mortal Wkly Rep. 2022 Feb 18;71(7):264-270. doi: 10.15585/mmwr.mm7107e3. https://pubmed.ncbi.nlm.nih.gov/35176002/
Prasad, S., Kalafat, E., Blakeway, H. et al. Systematic review and meta-analysis of the effectiveness and perinatal outcomes of COVID-19 vaccination in pregnancy. Nat Commun 13, 2414 (2022). https://doi.org/10.1038/s41467-022-30052-wNationella - internationella länkar
Nationellt vårdprogram för covid-19 läs här
Folkhälsomyndigheten https://www.folkhalsomyndigheten.se/smittskydd-beredskap/utbrott/aktuella-utbrott/covid-19/
ECDC https://www.ecdc.europa.eu/en
WHO https://www.who.int/emergencies/diseases/novel-coronavirus-2019?gclid=EAIaIQobChMIt5aezf_O6QIVxeAYCh1-0gjLEAAYASAAEgLAlvD_BwE
CDC https://www.cdc.gov/coronavirus/2019-nCoV/index.htmlACOG https://www.acog.org/covid-19
RCOG https://www.rcog.org.uk/en/guidelines-research-services/guidelines/coronavirus-pregnancy/
Läkemedelsverkets förteckning över
- godkända coronamediciner och medel under granskning på EMA läs här
- godkända Ccvid-19 vaccin och vaccin under granskning på EMA läs här
European Medical Agency EMA https://www.ema.europa.eu
Litteratur översikter
Bra referenser finns i översikterna i vårdprogram och på websidor
Living reviews:
Allotey J, Stallings E, Bonet M et al for PregCOV-19 Living Systematic Review Consortium. Clinical manifestations, risk factors, and maternal and perinatal outcomes of coronavirus disease 2019 in pregnancy: living systematic review and meta-analysis.
BMJ. 2020 Sep 1;370:m3320. doi: 10.1136/bmj.m3320 Läs här
Allotey J, Chatterjee S, Kew T,; PregCOV-19 Living Systematic Review Consortium. SARS-CoV-2 positivity in offspring and timing of mother-to-child transmission: living systematic review and meta-analysis. BMJ. 2022 Mai 07 16;376:e067696. doi: 10.1136/bmj-2021-067696.Terapi
Se Nationellt vårdprogram för covid-19 som iuppdateras regelbundet läs härSe även Läkemedelsverkets förteckning över
- godkända coronamediciner och medel under granskning på EMA läs här
- godkända Ccvid-19 vaccin och vaccin under granskning på EMA läs här
Winblad B, Nörby U. 22-05-04.Läkemedel vid covid-19 under graviditet. Janusinfo läs här
Risker för fostret
Khalil A, Blakeway H, Samara A, O'Brien P COVID-19 and stillbirth: direct vs indirect effect of the pandemic..Ultrasound in Obstet Gynecol. 2022 Mar;59(3):288-295. doi: 10.1002/uog.24846.
Shook LL, Sullivan EL, Lo JO et al. COVID-19 in pregnancy: implications for fetal brain development. Trends Mol Med. 2022 Feb 14;28(4):319–30. doi: 10.1016/j.molmed.2022.02.004. Epub ahead of print.
Placentapatologi
Hessami K, Aagaard K, Castro EC et al. Placental vascular and inflammatory findings from pregnancies diagnosed with coronavirus disease 2019 (COVID-19): A systematic review and meta-analysis. Am J Perinatol. 2022 Mar 3. doi: 10.1055/a-1787-7933 läs här
Schwartz DA; Avvad-Portari E, Babál P, et al. Placental Tissue Destruction and Insufficiency from COVID-19 Causes Stillbirth and Neonatal Death from Hypoxic-Ischemic Injury: A Study of 68 Cases with SARS-CoV-2 Placentitis from 12 Countries. Arch Pathol Lab Epub ahead of print 2022
Zaigham M, Gisselsson D, Sand A et al. Clinical-pathological features in placentas of pregnancies with SARS-CoV-2 infection and adverse outcome: case-series with and without congenital transmission. BJOG. 2022 Mar 3. doi: 10.1111/1471-0528.17132.
Sökord: covid-19, coronavirus, graviditet
Uppdaterad: 2023-10-22